비침습적 뇌 자극의 수면과 수면장애에 대한 효과
Effect of Non-Invasive Brain Stimulation on Sleep and Sleep Disorders
Article information
Trans Abstract
Non-invasive brain stimulation (NIBS), including transcranial magnetic and electrical stimulations, has recently been used to modulate sleep and treat sleep disorders. Herein, we reviewed studies that used NIBS to modulate sleep in healthy populations or patients with sleep disorders. Repetitive transcranial magnetic stimulation enhanced sleep slow oscillations and consistently improved subjective symptoms in patients with insomnia and restless legs syndrome. Transcranial electrical stimulation also increased slow-wave sleep in healthy populations and improved subjective sleep symptoms in patients with insomnia. Individualized NIBS and other NIBS techniques may be promising for treating sleep disorders, and future studies are warranted to determine optimal stimulation parameters and evaluate their long-term safety.
서 론
뇌 자극술은 신경과학의 발전에 따라서 활용도가 높아지고 있으며, 크게 뇌심부자극과 같은 침습적 자극술과 반복적 경두개 자기자극술(repetitive transcranial magnetic stimulation, rTMS) 또는 경두개 전기자극술(transcranial electric stimulation, TES)과 같은 비침습적 뇌 자극술(non-invasive brain stimulation, NIBS)로 구분된다[1]. NIBS는 비교적 안전하고 정확한 자극을 전달할 수 있어 우울증, 뇌전증, 만성통증, 그리고 수면과 같은 신경, 정신과적 질환에서 활용도가 높아지고 있다[2-5]. 본 종설에서는 대표적인 NIBS 방법에 대하여 알아보고, 그것이 정상 수면과 불면증을 포함하는 수면장애에서의 효과를 평가한 연구를 고찰해 보고자 한다.
본 론
NIBS의 종류
경두개 자기자극술(TMS)
TMS는 코일에 전류를 흘려 생기는 자기장 펄스가 두개골을 통과해 주로 대뇌피질, 때때로 피질하부위를 자극하여 자극부위의 신경조절을 유도하는 방법이다[1]. 코일을 흐르는 전류는 자기 에너지로 변환된 후 신경세포에서 유도전류로 전환되게 된다. 대뇌피질 흥분을 평가하기 위하여 한번 또는 쌍자극(paired-pulse)을 줄 수 있으며, 특정 주파수로 반복적으로 자극을 주는 rTMS는 대뇌피질 흥분을 증가, 또는 감소시킬 수 있어 신경조절 목적으로 사용할 수 있다. 보통 1 Hz 미만의 낮은 주파수로 반복적으로 자극을 주었을 때 신경흥분을 억제할 수 있으며, 5 Hz 이상의 높은 주파수로 반복적으로 자극을 주었을 때 신경흥분을 높일 수 있다[6]. rTMS에서 네비게이션 장비를 사용하는 경우 1 mm 해상도로 자극을 줄 수 있으며, 자극 강도는 말초 근육자극을 주는 근육유발 전위의 비율(%)로 정한다[7,8].
경두개 전기자극술(TES)
TES는 낮은 전류를 두피에 흘려주는 것이고 직류전류를 사용하는 경두개직류전기자극술(transcranial direct current stimulation, tDCS)과 교류전류를 사용하는 경두개교류전기자극술(transcranial alternating current stimulation, tACS)이 있다[1]. 일반적으로 TMS에 비하여 TES가 가격이 저렴하고 휴대용으로 사용이 편하며 부작용도 적은편이라 유용하다[8,9].
tDCS는 배터리에서 수 밀리암페어를 전달하는데, TMS와는 달리 직접 신경흥분을 일으키지 않고 신경막전위(neural membrane potential)를 바꿔 대뇌피질 흥분을 변화시킨다고 알려져 있다[10]. 전류는 양극(anode)에서 음극(cathode)으로 흐르는데 tDCS 양극자극을 주면 탈분극이 되어 대뇌피질 흥분이 증가하고 음극자극을 주면 과분극(hyperpolarization)이 되어 대뇌피질 흥분이 억제된다. 보통 10분 정도 tDCS 자극을 주면 효과가 1시간 가까이 지속된다고 알려져 있으며, 반복적인 자극을 통해 치료효과가 지속될 수 있다고 알려져 있다[10,11]. 최근에는 양극 주변으로 4개의 음극을 배치하여 국소적으로 전기자극을 줄 수 있는 고해상도 경도개 직류자극술(high-definition tDCS, HD-tDCS) 방법도 사용되고 있다. tACS는 교류전류를 통해서 뇌 진동의 강도(power)와 상(phase)을 조절한다고 알려져 있다. 그 기전으로는 0.1-80 Hz 자극을 주면 신경내부 진동이 외부와 동기화되어 N-methyl-D-aspartate (NMDA) 수용체 가소성(plasticity)을 조절하는 것으로 알려져 있다.
건강한 대상자에서 NIBS의 수면조절 효과
rTMS의 수면조절 효과
rTMS는 대뇌피질 각성을 조절하고 시상하부-뇌하수체-부신 축(Hypothalamus-Pituitary-Adrenal [HPA] axis), 자율신경계에 영향을 주어 수면을 조절할 수 있으며, 멜라토닌과 가바 분비를 촉진할 수 있다[2]. 수면 중 rTMS 자극이 수면에 어떠한 영향이 있는지를 평가하기 위해 정상인 6명에서 N2 수면 중 정중앙(Cz) 부위에 0.8 Hz, 최대자극의 60%로 40×4 펄스 자극을 주었을 때 느린파(slow wave)가 유도되는 것을 확인하였다[12]. 각성 중에 동일한 rTMS 자극을 줘도 변화가 나타나지 않아서 각성 정도에 따라서 반응이 달라질 수 있으며, 자극을 머리 뒤쪽에서 줄수록 서파 전위가 커져 자극 위치에 따라서도 반응이 달라질 수 있음을 확인하였다. 입면 전 5 Hz rTMS 자극을 준 후 처음 나타나는 NREM 수면의 변화를 확인한 연구에서는 강한 자극을 줄수록 국소적인 서파 생성이 증가됨을 확인하였다[13].
TES의 수면조절 효과
젊은 남성 30명에서 서파수면 중 tDCS 자극을 양측 전두엽 부위에 0.26 mA/cm2 세기로 30분간 반복적으로 주었을 때, 자극 후 서파수면이 더 지속되었으며 서술기억(declarative memory) 보존이 증가하였음을 확인하였다. 또한 각성 중 동일한 자극을 주었을 때는 변화를 확인하지 못하였다[14]. 저주파에서 교류전류와 직류전류 오프셋(offset)의 조합을 저주파 경두개직류자극(slow oscillatory tDCS, so-tDCS)이라고 하는데, 이를 이용하여 수면조절에 사용한 연구가 보고되었다. 한 연구에서 13명의 젊은 남성에서 N2 수면에 맞춰 0.75 Hz so-tDCS 자극을 전두엽(F3, F4) 위치에 줬더니 서파수면이 늘어났고 서술기억(declarative memory)이 호전되었으나 절차기억(procedural memory)의 변화는 없었다[15]. 노령인구에서도 동일한 자극을 90분 낮잠 중 주었을 때 서파강도가 증가하고 사진을 이용한 시공간 기억이 촉진됨을 확인하였으나 단어기억의 차이는 없었다[16]. 하지만, tDCS 자극이 수면과 기억에 대한 효과가 연구마다 일관되게 나타나지는 않았다. 동일한 방법으로 0.75 Hz so-tDCS 자극을 노령 인구에서 주었을 때 수면단계에 유의미한 변화가 없었고 서술기억, 절차기억의 차이도 확인하지 못하였다[17]. 젊은 정상인에서는 수면구조의 변화를 확인하지 못하였으며 기억고정(memory consolidation)의 차이도 확인하지 못하였다[18].
HD-tDCS가 주관적 수면과 기능성 자기공명영상(magnetic resonance imaging, MRI)에 미치는 변화를 평가하기 위해 좌측 전배외측전전두피질(dorsolateral prefrontal cortex, DLPFC)에서 매일 25분간 2주간 자극을 준 자극군 16명과 대조군 15명에서 자극 전후 수면의 질을 피츠버그 수면의 질 평가척도(Pittsburg Sleep Quality Index, PSQI) 설문지로 평가한 결과, 자극군과 대조군 사이 차이는 없었지만 수면시간이 자극군에서만 유의미하게 증가하였다[19]. 또한 멍한 상태에서 나타나는 디폴트 모드 네트워크의 상관성 정도가 자극군에서만 감소하였고 PSQI 점수 변화와 상관관계가 있음도 확인하였다. Frase 등[20]은 5일 동안 수면다원검사를 하면서 양측 전두엽 부위에 양극, 음극, 그리고 위자극을 주어 세 군의 효과를 비교하였는데, 양극 자극 후 뇌파에서 감마파가 증가하고 수면시간이 25분 감소하며 수면효율이 떨어졌으나, 위자극 또는 음극 자극 후 수면시간이 증가하지 않았다.
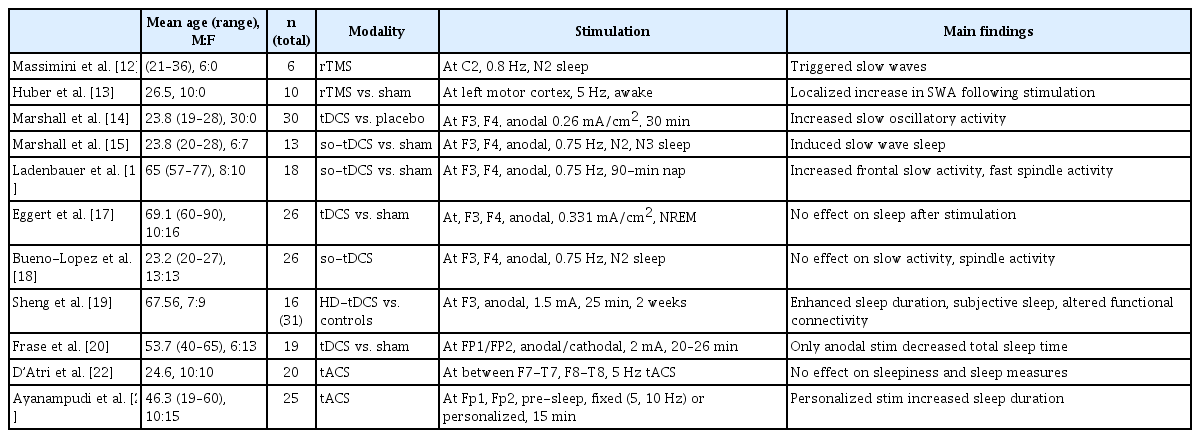
tACS를 이용한 연구는 최근 보고되고 있다. 건강한 대상자 30명에서 5 Hz의 tACS를 DLPFC에 주고 15분 후 낮잠을 자도록 하였을 때 뇌파에서 1-7 Hz 저주파 강도가 증가하였고 입면기간이 감소하였다[21]. 하지만, 5 Hz의 tACS를 양측 전두엽(F7, F8)에서 측두엽(T7, T8)으로 10분간 준 후 수면에 들게 하였을 때 전반적 수면다원검사 및 뇌파분석 지표 변화를 확인하지 못하였다[22]. 다만 자극 중 각성 뇌파에서 세타파 증가를 보인 반응군만 따로 분석하였을 때 서파수면의 증가를 확인하였다. 최근 5 Hz 고정 주파수가 아닌 개인 뇌파를 측정하여 개별화된 주파수의 tACS 자극을 준 연구에서는 개별화된 자극을 준 군에서만 수면시간이 대조군에 비해 22분, 고정자극군에 비해 19분 증가하는 것을 확인하였다[23]. 총 511명의 건강한 대상자와 452명의 환자군을 비교한 40개 연구를 모아 분석한 체계적 문헌고찰 논문에 따르면 NIBS 후 주관적인 증상은 호전을 보였으나 뇌파검사 및 수면다원검사결과의 차이는 연구마다 다르게 보고되었다(Table 1) [24].
불면증 환자에서 NIBS의 효과
불면증 환자는 과각성상태(hyperarousal state)를 보이며, 수면 중에는 시상활동이 증가되어 있는 반면에 각성 중에는 전전두엽 활동이 감소되어 있다[25]. NIBS를 이용하여 대뇌피질 흥분을 조절하여 불면증 증상을 감소시키기 위한 연구가 보고되었다.
불면증에서 TMS의 효과
불면증에서 rTMS 자극의 효과를 다른 치료와 비교하여 평가하기 위해 120명의 일차성불면증 환자를 세 그룹(rTMS 자극군, 약물치료군, 인지행동치료군)으로 나누어 2주간 치료를 시행한 후 수면다원검사와 수면설문지검사를 추적 시행하였고, 치료 3개월 후 불면증이 지속되는지 여부를 확인하였다. rTMS는 1 Hz 저주파 자극으로 2주간 시행하였고 약물 치료군에서는 2주간 에티졸람 2 mg을 투여하였다. 수면시간과 수면효율은 모든 군에서 호전되었으나 약물치료군에서 호전 정도가 가장 컸으며 rTMS 자극군이 그 다음이었다. 하지만 N3 수면과 렘수면은 rTMS 자극군에서 가장 많이 증가하였으며, 3개월 후 불면증이 지속되는 환자 비율은 rTMS 자극군에서 가장 적었고 약물치료군에서 가장 높았다[26]. 또한 혈중 코티솔과 갑상선자극호르몬과 갑상선호르몬이 감소하는 것을 통해 rTMS 자극이 HPA 축에 영향을 줌을 확인하였다. rTMS가 불면증을 개선시키는 기전을 대뇌신경전달물질 분석을 통해 규명하고자 한 연구가 있다. 한 연구는 불면증 환자 32명을 대상으로 DLPFC에 1 Hz 자극을 2주간 주어서 주관적 증상과 대뇌피질 각성을 반영하는 혈장지표(brain-derived neurotrophic factor [BDNF], gamma-aminobutyric acid [GABA]) 농도변화를 확인하였다[27]. rTMS 자극 후 PSQI 설문점수가 감소하였고 혈중 BDNF, GABA가 증가하였으며 증가된 정도는 PSQI 점수와 음의 상관성을 보였다. 다른 연구는 H1 자기공명분광법(MR spectroscopy)을 통해 40명의 만성불면증 환자에서 rTMS 자극 이후 뇌내 대사물질을 분석하였고, 가바(GABA+/Cr) 농도가 자극군에서만 증가됨을 확인하였다[28].
뇌파 연결성 분석을 통해 불면증 환자에서 rTMS 자극의 효과를 규명한 연구도 보고되었다. 한 연구에서는 후두정엽(posterior parietal cortex)에 1 Hz rTMS 자극을 2주간 주는 것이 수면과 뇌파 연결성에 미치는 영향을 평가하였다. 자극 직후 시행한 설문지에서 수면효율, 주간졸림, 불면증상이 모두 좋아졌고 1달 이후까지 증상이 지속되었다. 또한 자극 후 뇌파 연결성이 증가되었는데 자극 전 증가해 있었던 연결성은 감소하고 감소해있던 연결성이 증가하였다[29]. 저주파 rTMS 자극 전 베타와 알파밴드의 전전두엽과 전두엽, 대뇌섬과, 변연피질(limbic cortex) 간 연결성 저하가 자극 후 PSQI 점수호전과 연관성을 보여 rTMS 치료반응을 예측하는 인자로 사용할 수 있음을 보여준 연구도 있었다[30]. 다른 연구에서는 좌측 DLFPC에 1 Hz rTMS 자극을 준 후 기능적 MRI를 이용하여 대뇌연결성을 분석하였고, 자극 전 증가한 좌측 DLPFC와 우측 위이마고랑(superior frontal gyrus) 연결성이 자극 후 정상화되며 좌측 해마와 연결성도 정상화됨을 확인하였다[31].
주요우울장애를 가진 환자 중 대부분에서 수면장애가 있으며 불면증 동반여부는 우울증상 정도와 연관있는 것으로 보고되었다[32,33]. 우울증 치료에서 rTMS는 효과적인 방법으로 증명되었기 때문에 불면증 증상 호전에 우울증 개선이 영향을 주었을 것으로 생각된다. 한 연구에서는 주요우울장애가 동반된 21명의 환자에서 10 Hz rTMS를 좌측 DLPFC에 주고 치료 전후 PSQI와 우울증 증상설문지를 시행하였을 때 PSQI 점수와 우울증 점수의 감소를 확인하였다. 이 연구에서는 하위집단 분석을 통해 우울증 점수 개선이 없는 환자에서도 PSQI 점수 감소가 있었고, PSQI 점수 개선이 없었던 환자에서도 우울증 점수가 감소됨을 확인하였다[34]. 또한 우울증 개선 이후에도 72% 환자에서는 불면증상이 지속된다는 보고가 있어[35] rTMS 치료 후 불면증과 우울증은 독립적으로 호전됨을 유추할 수 있다.
메타연구에서는 총 28개 연구에서 2357명의 성인 불면증 환자를 대상으로 rTMS의 수면개선 효과를 분석하였다. 위 자극과 비교하여 자극군에서 유의미한 수면개선 효과가 있었고(standardized mean difference [SMD] -2.31, 95% confidence interval [CI] -2.95 - -1.66), 약물치료 등 다른 치료에 추가하여 rTMS를 시행하였을 때 그렇지 않은 군에 비해 수면이 개선되었다(SMD -1.44, 95% CI: -2.0 - -0.88). 또한 다른 치료와 비교해서도 rTMS 자극군에서 유의미한 수면 개선을 보여(SMD -0.63, 95% CI: -1.22 - -0.04) 불면증에서 rTMS가 안전하고 효과적인 치료방법임을 보고하였다[36]. rTMS 자극효과에서 위약효과(placebo-effect)가 얼마나 되는지 평가하기 위해 9개 연구에서 580명 환자를 대상으로 분석하여 자극 효과의 73.5% 가량이 위약효과임을 보고한 연구도 있다[37].
불면증에서 TES의 효과
Frase 등[38]이 정상군을 대상으로 시행한 프로토콜과 동일한 방법으로 불면증 환자 19명을 대상으로 tDCS 자극을 주었을 때 양극, 음극, 그리고 위자극에 따른 수면시간, 수면효율과 뇌파의 차이를 확인하지 못하였다. 국내에서 시행된 무작위 이중맹검 임상시험은 군당 2-3명으로 환자 수가 적 만, 총 수면시간과 수면효율이 양극자극군에서는 전부 호전되었고, 음극자극 또는 위자극군에서는 절반만 호전을 보였으며 한달 째 증상 호전 비율은 양극자극군에서 가장 높음을 확인하였다[39].
최근에는 tDCS를 이용하여 다른 질환과 동반된 불면증 조절에 대한 연구가 보고되고 있다. 주요우울증이 동반된 불면증 환자 47명에서 이중맹검 무작위배정 tDCS 치료를 DLPFC에 2 mA로 30분에 걸쳐 20세션을 시행하였을 때 위자극군에 비하여 자극군에서 우울증의 개선뿐만 아니라 PSQI 총점과 그 중 특히 수면시간과 수면의 질을 반영하는 점수가 호전됨을 확인하였다. 또한 자극군에서 수면다원검사결과 총 수면 시간과 수면효율이 증가됨을 확인하였다[40]. 외상성뇌손상 환자 중 불면증이 있는 환자 60명을 대상으로 우측 DLPFC (F4) 위치에 1.5 mA로 15분간 총 3주간 15세션을 시행하였을 때, 위약군에 비해 자극군에서 PSQI 점수 감소가 6주까지 지속되었고 젊은 남자에서 그 효과가 더 컸다[41]. 다발성경화증 환자 7명에서 무작위로 tDCS 양극자극을 좌측 DLPFC에 주었을 때 주관적 주간졸림을 나타내는 엡워스 수면척도는 자극군에서만 감소하였으나 액티그래피로 측정한 수면지표의 차이는 확인하지 못하였다[42].
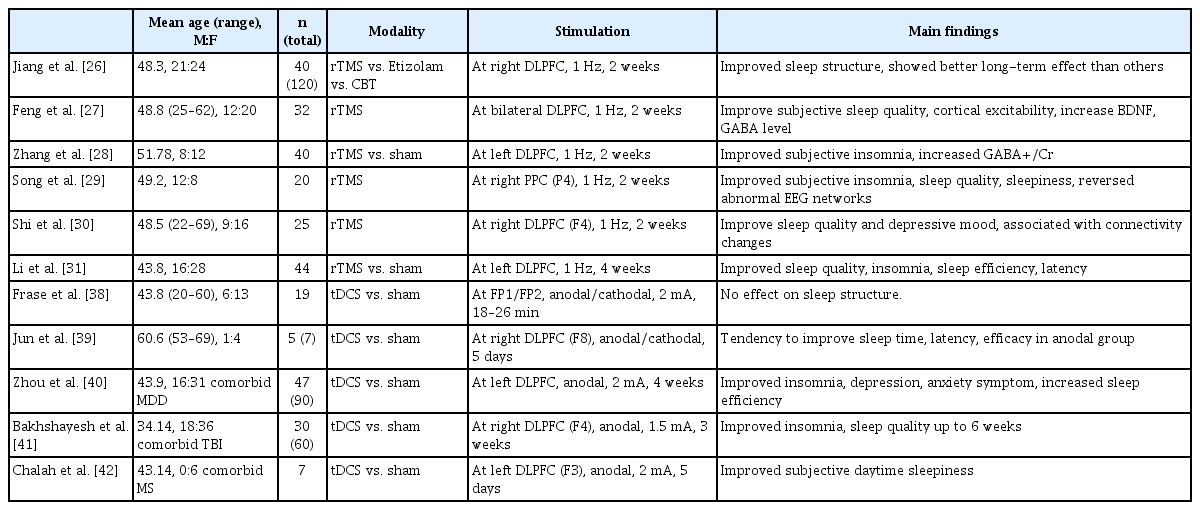
메타연구에서는 27개의 rTMS 연구와 16개의 TES 연구를 모아 분석하였을 때 두 군 모두에서 PSQI 점수의 유의미한 감소를 확인하였고 rTMS에서 감소폭(-4.08, 95% CI: -4.86 - -3.30)은 TES (-1.17, 95%CI: -1.98 - -0.36)에 비해 컸다. 수면다원검사 지표를 보았을 때 TES 치료군은 수면시간, 수면 효율에서 차이가 없었던 반면에, rTMS 치료군에서는 수면시간, 수면효율이 증가하고 수면잠복기, 입면 후 각성시간이 감소하였다. 또한 rTMS의 효과는 성별, 치료 세션 수와 펄스 수, 그리고 치료 기간과 연관되어 있었다(Table 2) [43].
기타 수면질환에서 NIBS의 효과
폐쇄성수면무호흡증(Obstructive sleep apnea, OSA)
OSA 환자에서 NIBS는 턱끝혀근(genioglossus muscle) 흥분을 조절할 수 있는 운동신경영역을 자극효과를 평가한 연구가 보고되었으나 유의미한 개선을 확인하지 못하였다. 횡경막신경자극 치료를 받고있는 OSA 환자 10명에서 턱끝혀근 근전도를 변화시키는 위치에 25 Hz rTMS 자극을 200 msec 동안 각성 중 주었을 때 자극을 주지않은 군과 비교하여 상기도 기류 등 기계적 성질에 변화를 주지 못하였다[44]. 같은 방법으로 비렘수면 중 rTMS 자극을 주었을 때도 상기도 기류를 호전시키지 못하였으나 자극에 따른 각성은 없었다[45]. 현재까지 수면무호흡증에 대한 TES 연구는 보고되지 않았다.
하지불안증후군(Restless legs syndrome, RLS)
RLS에서 NIBS를 적용한 연구는 주로 하지 운동 및 감각영역을 자극하는 효과를 평가하였다. 한 연구에서 RLS 환자 19명을 대상으로 5 Hz rTMS 자극을 좌측 운동보조영역(supplementary motor area)에 10세션을 총 1달간 시행한 이중맹검 연구에서 자극군 11명과 위약군 8명을 비교하였다. 자극 5세션 후부터 두 군 모두에서 국제하지불안척도(International Restless Legs Scale) 점수가 감소하였으나 자극군에서 그 정도가 더 크게 나타났고, 모든 세션이 종료된 후에는 자극군에서만 유의미한 증상 감소가 있었다[46]. 다른 연구에서는 15명의 하지불안증후군 환자에서 rTMS를 하지 운동영역에 위치하여 5 Hz 자극을 2주간 주어 14명의 대조군과 비교하여 분석하였을 때 주관적 증상이 호전되었고, 기능적 MRI 결과 RLS 환자에서 rTMS 이후에 운동체성감각, 시각피질부위에 주파수 파동의 진폭(amplitude of low frequency fluctuation)이 증가하였다[47]. 또한 중국 연구에서 14명의 하지불안증후군 환자에서 15 Hz rTMS 자극을 다리 운동피질부위에 18일간 14세션으로 주었을 때 운동증상, 수면의 질과 불안증상이 개선되었고 그 효과가 2달 동안 지속되었다[48]. 운동영역이 아니라 감각-운동 네트워크 조절을 위해 운동체성감각 피질(sensorimotor cortex) 에 자극을 준 연구도 보고되었다. 이 연구에서는 한 세션의 1 Hz rTMS를 좌측 운동체성감각피질에 50번 자극을 준 것으로도 RLS 환자 13명에서 입면과 수면유지 등 주관적 수면증상이 호전되었다[49].
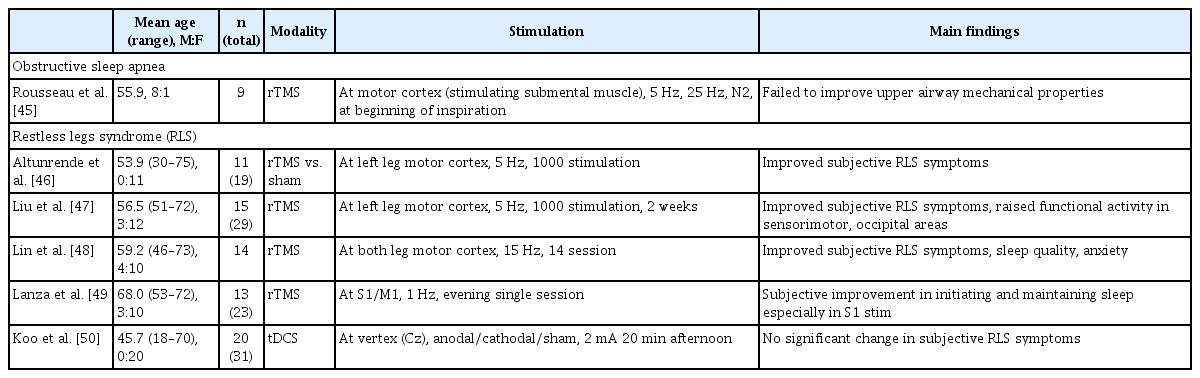
RLS 환자를 대상으로 TES 효과를 평가한 연구는 하나만 보고되었다. 국내에서 31명의 여성 RLS 환자를 대상으로 tDCS를 정중앙(Cz) 부위에 총 5세션(오후 5-7시, 2 mA, 20분간) 동안 자극을 주는 2주간 무작위 이중맹검연구 결과 양극자극, 음극자극군과 대조군간 PSQI 총점 및 뇌파분석결과 군간 유의미한 차이를 확인하지는 못하였다(Table 3) [50].
결 론
NIBS는 뇌 흥분도, 네트워크 조절 및 신경조절물질 변화를 통해 수면에 영향을 줄 수 있다. 현재 불면증에서 NIBS의 효과가 일관되게 보고되지만, 자극 부위, 강도 등이 연구마다 다르게 시행되어서 추후 프로토콜의 통일화 또는 개별화된 프로토콜을 적용하는 연구가 필요하겠다. 수면무호흡증에서 NIBS의 유의미한 효과는 보고되지 않았으나 다양한 표현형에 따라 효과에 차이가 있을 수 있어서 향후 추가 연구가 필요하겠다. 하지불안증후군에서 rTMS의 효과는 비교적 일관되게 보고되었으나 운동 또는 운동체성감각영역 자극에 따른 차이를 비교해 더 효과적인 프로토콜 정립이 필요하겠다. 더불어 위약효과가 불면증의 경우 73.5%로 보고되고 있으며 자극 도구, 위치, 프로토콜에 따른 결과 차이가 많아 수면 및 수면 장애를 대상으로 하는 NIBS 연구 시행 및 해석에 주의가 필요하다. 또한 국소적인 자극을 줄 수 있는 HD-tDCS와 신경조절에 유용한 tACS의 경우 수면장애 환자에 적용한 연구가 부족하여 향후 추가적인 연구가 필요하겠다.
Notes
The authors have no potential conflicts of interest to disclose.
Author Contributions
Conceptualization: all authors. Data curation: Jung-Ick Byun. Funding acquisition: Jung-Ick Byun. Investigation: Jung-Ick Byun. Supervision: Won Chul Shin, Ki-Young Jung. Validation: Won Chul Shin, Ki-Young Jung. Writing—original draft: Jung-Ick Byun. Writing—review & editing: Won Chul Shin, Ki-Young Jung.
Funding Statement
This work was supported by the National Research Foundation of Korea (NRF) (No. NRF-2020R1C1C1013160).
Acknowledgements
None